Uma nova pesquisa da Michigan State University publicada em março de 2026 acaba de revelar o mecanismo molecular exato que faz com que a cocaína "reprograme" o cérebro — e explica por que tantas pessoas recaem mesmo após anos de abstinência. Os protagonistas dessa descoberta são duas proteínas até então pouco compreendidas: a DeltaFosB e a calreticulina. Juntas, elas alteram a expressão de mais de 1.400 genes nos neurônios do sistema de recompensa, criando uma espécie de "memória permanente" do prazer da droga que persiste por meses ou até anos.
Neste artigo, vamos mergulhar fundo na neurociência do vício, explicar como a cocaína sequestra o sistema de recompensa do cérebro, detalhar o papel revolucionário da DeltaFosB e da calreticulina, e discutir como essa descoberta pode levar a tratamentos mais eficazes contra a dependência química.
O Sistema de Recompensa: A Máquina de Prazer do Cérebro
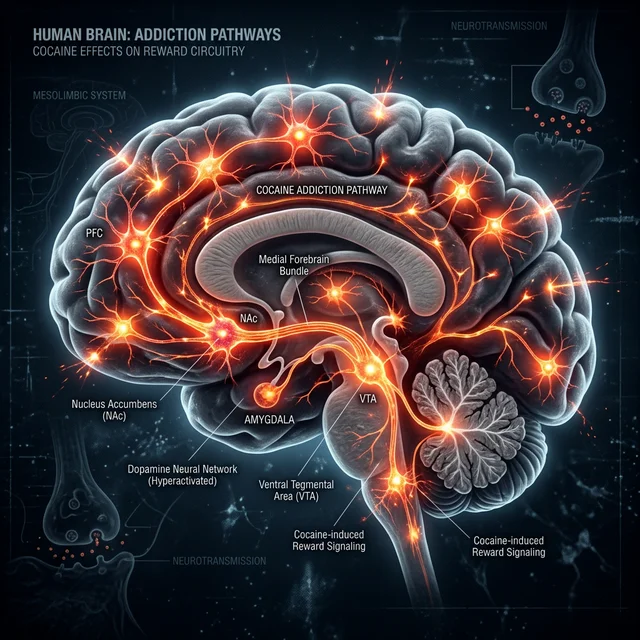
Para entender como a cocaína reprograma o cérebro, primeiro precisamos compreender o sistema de recompensa — um circuito neural sofisticado que evoluiu ao longo de milhões de anos para nos motivar a buscar comportamentos essenciais para a sobrevivência: comer, beber água, fazer sexo e criar vínculos sociais.
O sistema de recompensa é composto por três regiões cerebrais principais:
- Área Tegmental Ventral (VTA): A "fábrica de dopamina" do cérebro. Neurônios aqui produzem e liberam dopamina.
- Nucleus Accumbens (NAc): O "centro de prazer". Recebe a dopamina da VTA e gera a sensação de recompensa e motivação.
- Córtex Pré-Frontal (PFC): O "juiz". Interpreta as informações do NAc e toma decisões sobre buscar ou não buscar uma recompensa.
Quando você come algo delicioso ou recebe um abraço, a VTA libera uma quantidade moderada de dopamina no NAc, gerando uma sensação agradável que o motiva a repetir o comportamento. É um sistema elegante e bem calibrado.
A cocaína, no entanto, explode esse sistema com uma força brutal.
Como a Cocaína Sequestra o Sistema Dopaminérgico
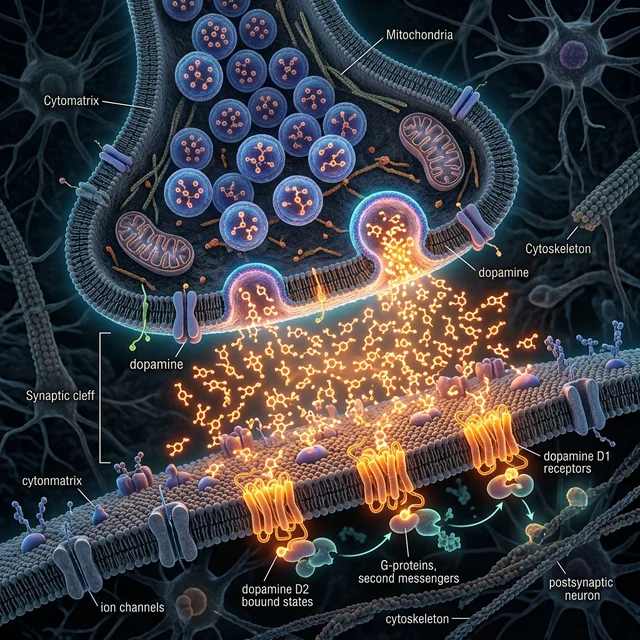
Em condições normais, depois que a dopamina envia seu sinal na sinapse, ela é recapturada pelos neurônios pré-sinápticos através de uma proteína chamada transportador de dopamina (DAT). Esse mecanismo de "reciclagem" garante que os níveis de dopamina sejam controlados e que os sinais de prazer tenham início e fim definidos.
A cocaína age como um bloqueador do DAT. Ao se ligar ao transportador, ela impede que a dopamina seja recapturada, fazendo com que quantidades massivas do neurotransmissor se acumulem na fenda sináptica. O resultado é uma inundação de dopamina 2 a 10 vezes maior do que qualquer recompensa natural — gerando uma euforia intensa que nenhuma experiência biológica normal pode igualar.
| Estímulo | Aumento de Dopamina | Duração |
|---|---|---|
| Comida saborosa | ~50% acima do basal | 10-20 min |
| Sexo | ~100% acima do basal | 15-30 min |
| Música favorita | ~20% acima do basal | 5-15 min |
| Nicotina | ~150% acima do basal | 20-40 min |
| Cocaína | 350-1000% acima do basal | 15-30 min |
| Metanfetamina | 1200% acima do basal | 6-12 horas |
O problema não é apenas a intensidade do prazer — é o que acontece depois.
DeltaFosB: O "Interruptor Molecular" da Dependência

A grande revelação da pesquisa de 2026 está na proteína DeltaFosB (ΔFosB). Diferente da maioria das proteínas cerebrais que são produzidas e degradadas em questão de horas, a DeltaFosB é excepcionalmente estável — ela se acumula nos neurônios do Nucleus Accumbens e pode persistir por semanas ou meses após a última exposição à droga.
O Que a DeltaFosB Faz
A DeltaFosB é um fator de transcrição — uma proteína que se liga ao DNA e controla quais genes são ativados ou silenciados. Quando a cocaína causa a acumulação crônica de DeltaFosB, ela:
- Aumenta a expressão de receptores de glutamato (GluR2): Tornando os neurônios mais sensíveis a sinais excitatórios relacionados à recompensa
- Modifica a estrutura das sinapses: Promove o crescimento de espinhas dendríticas — as "antenas" que recebem sinais de outros neurônios — especificamente nos circuitos de recompensa
- Reduz a expressão de dinorfina: Um neurotransmissor que normalmente desacelera o sistema de recompensa, criando um "freio" natural contra o excesso de prazer
- Altera a sensibilidade à dopamina: Aumentando a resposta do cérebro a pistas ambientais associadas à droga
O resultado é um cérebro que literalmente se recabeia para buscar obsessivamente a cocaína, mesmo quando a pessoa conscientemente não quer usá-la.
Calreticulina: A Peça que Faltava no Quebra-Cabeça
A grande novidade de 2026 é a descoberta do papel crucial da calreticulina — uma proteína até então conhecida apenas por seu papel no processamento de outras proteínas no retículo endoplasmático. A equipe da Michigan State University descobriu que a calreticulina atua como um "cofator" da DeltaFosB, amplificando e estabilizando seus efeitos epigenéticos.
Especificamente, a calreticulina:
- Ajuda a DeltaFosB a se ligar mais firmemente ao DNA
- Protege a DeltaFosB da degradação, prolongando seus efeitos
- Facilita a modificação de histonas — as proteínas que "empacotam" o DNA, controlando quais genes são acessíveis para transcrição
- Afeta mais de 1.400 genes no Nucleus Accumbens — quatro vezes mais do que se acreditava anteriormente
A Neurobiologia da Recaída
A recaída é, talvez, o aspecto mais devastador e incompreendido da dependência de cocaína. Dados clínicos mostram que 40 a 60% dos dependentes de cocaína recaem nos primeiros 12 meses após o tratamento, e muitos o fazem após anos de sobriedade. Agora, graças à pesquisa sobre DeltaFosB e calreticulina, entendemos por quê.
O Ciclo da Recaída em 5 Etapas
- Pistas ambientais: Uma música, um lugar, um cheiro ou uma pessoa associada ao uso desencadeia uma resposta do circuito de recompensa alterado
- Ativação do NAc modificado: A DeltaFosB criou conexões neuronais extra-sensíveis que respondem intensamente a essas pistas
- Craving intenso: O cérebro gera um desejo avassalador pela droga que é percebido como uma "necessidade" biológica
- Falha do controle executivo: O PFC — já enfraquecido pelo uso crônico — não consegue "vetar" o impulso do NAc
- Uso ou resistência agonizante: A pessoa usa a droga ou resiste com esforço extraordinário que consome grande parte de seus recursos mentais
Quanto Tempo as Alterações Persistem?
Uma das descobertas mais impactantes é a durabilidade das modificações induzidas pela DeltaFosB-calreticulina:
| Alteração | Persistência após última dose | Implicação |
|---|---|---|
| Espinhas dendríticas extras no NAc | 1-4 meses | Hipersensibilidade a pistas da droga |
| Expressão alterada de GluR2 | 2-6 meses | Resposta exagerada a estímulos de recompensa |
| Modificações epigenéticas (histonas) | 6-12+ meses | Vulnerabilidade de longo prazo à recaída |
| Redução da matéria cinzenta no PFC | 12-24 meses (parcial) | Menor autocontrole e tomada de decisão |
| Sensibilização cruzada | Anos | Risco aumentado com outras substâncias |
Esses dados explicam por que a dependência de cocaína é classificada como uma doença crônica do cérebro e não como uma "fraqueza moral" ou "falta de força de vontade".
Novos Caminhos Para o Tratamento
A identificação do papel da calreticulina abre portas para estratégias terapêuticas completamente novas. Historicamente, o tratamento da dependência de cocaína tem sido um dos maiores desafios da psiquiatria — não existem medicamentos aprovados especificamente para isso (ao contrário do alcoolismo e da dependência de opioides).
Terapias em Desenvolvimento (2026-2030)
Inibidores de Calreticulina: Moléculas que bloqueiam a interação entre calreticulina e DeltaFosB poderiam prevenir a "reprogramação" genética sem afetar a função normal da calreticulina em outras células. Três candidatos estão em fase pré-clínica.
Terapia Epigenética Direcionada: Usando ferramentas CRISPR-dCas9 modificadas para reverter as alterações nas histonas dos genes-alvo da DeltaFosB, restaurando padrões normais de expressão gênica.
Vacina Anti-Cocaína: Já em fase 2 de testes clínicos, a vacina TA-CD gera anticorpos que se ligam à molécula de cocaína no sangue, impedindo-a de cruzar a barreira hematoencefálica.
Estimulação Magnética Transcraniana (TMS): Aplicação de campos magnéticos pulsantes sobre o PFC para fortalecer os circuitos de controle executivo enfraquecidos pelo uso crônico.
Terapia com Psilocibina: Ensaios clínicos em universidades dos EUA e Europa estão testando microdoses de psilocibina como adjuvante ao tratamento psicoterapêutico, com resultados promissores na redução do craving.
Os Números da Dependência de Cocaína no Mundo
O contexto global ilustra a urgência desta pesquisa:
- 21 milhões de pessoas usam cocaína regularmente no mundo (UNODC, 2025)
- O Brasil é o 2º maior mercado consumidor de cocaína do mundo, atrás apenas dos EUA
- O custo global da dependência de cocaína excede US$ 180 bilhões anuais em saúde, justiça criminal e perda de produtividade
- Apenas 25% dos dependentes que buscam tratamento completam os programas de reabilitação
- A taxa de recaída em 5 anos é de 80-90% sem tratamento farmacológico eficaz
O Impacto no Brasil
O Brasil enfrenta uma crise particular com a cocaína e seus derivados, especialmente o crack. A descoberta da via DeltaFosB-calreticulina tem implicações diretas para:
- CAPS-AD (Centros de Atenção Psicossocial): Podem incorporar estratégias de prevenção de recaída baseadas na neurociência molecular
- Políticas públicas: Evidência científica robusta de que dependência é doença cerebral pode influenciar legislação e investimentos em saúde
- Pesquisa nacional: Instituições como FIOCRUZ, UNIFESP e USP podem desenvolver pesquisas translacionais para adaptar os achados ao contexto brasileiro
- Destigmatização: Compreender que a recaída tem bases moleculares específicas ajuda a combater o preconceito contra pessoas com dependência
Cérebro vs. Vontade: O Que a Ciência Realmente Diz

Uma das questões mais debatidas na ciência da dependência é: "Se o vício é uma doença do cérebro, a pessoa perde todo o controle?" A resposta é mais nuançada do que "sim" ou "não".
A pesquisa de 2026 mostra que a cocaína não elimina a capacidade de escolha — ela distorce profundamente o campo de decisão. É como jogar um jogo com dados viciados: você ainda faz escolhas, mas as opções estão massivamente inclinadas a favor do comportamento aditivo. O PFC ainda funciona, mas está lutando contra um NAc recabeado e hiperestimulado.
Comparação com Outras Substâncias
A DeltaFosB é induzida por diversas drogas, mas em diferentes graus:
| Substância | Nível de DeltaFosB induzido | Velocidade de acumulação | Dificuldade de tratamento |
|---|---|---|---|
| Álcool | Moderado | Lenta (meses) | Moderada (naltrexona disponível) |
| Cannabis | Baixo | Lenta (meses) | Baixa a moderada |
| Nicotina | Moderado | Rápida (semanas) | Moderada (vareniclina disponível) |
| Cocaína | Alto | Rápida (semanas) | Alta (sem medicamento aprovado) |
| Metanfetamina | Muito alto | Muito rápida (dias) | Muito alta |
| Opioides | Moderado-Alto | Moderada | Alta (mas buprenorfina existe) |
Perguntas Frequentes
A cocaína causa danos permanentes ao cérebro? As alterações epigenéticas podem durar meses a anos, mas evidências sugerem que muitas são reversíveis com o tempo e tratamento adequado. A neuroplasticidade do cérebro permite recuperação significativa, embora isso possa levar anos.
Um único uso de cocaína pode causar dependência? Um único uso não é suficiente para acumular níveis significativos de DeltaFosB. Contudo, o uso repetido — mesmo que relativamente espaçado — cria um efeito cumulativo que pode levar à dependência.
A descoberta da calreticulina muda o tratamento atual? Ainda não diretamente, pois os inibidores estão em fase pré-clínica. Mas a descoberta valida abordagens de prevenção de recaída baseadas em neuroplasticidade e pode levar a medicamentos aprovados em 5-10 anos.
Por que não existe uma pílula contra a cocaína? A cocaína afeta múltiplos sistemas neurotransmissores simultaneamente (dopamina, serotonina, noradrenalina), tornando difícil encontrar um único alvo farmacológico. A calreticulina pode ser esse alvo.
A maconha ou o álcool causam alterações semelhantes? Sim, mas em escala muito menor. A cannabis induz níveis baixos de DeltaFosB, enquanto o álcool produz níveis moderados. A cocaína e a metanfetamina são as substâncias que mais intensamente ativam essa via molecular.
Exercício físico pode ajudar na recuperação? Sim, há evidências robustas. Exercício aeróbico regular estimula a produção de BDNF (fator neurotrófico derivado do cérebro), que promove neuroplasticidade e ajuda a restaurar circuitos danificados pela cocaína. Estudos mostram que 30 minutos de exercício intenso podem reduzir o craving em até 40%.
Neuroplasticidade: A Esperança da Recuperação
Apesar da gravidade das alterações causadas pela DeltaFosB e calreticulina, o cérebro humano possui uma capacidade extraordinária de se reparar. A neuroplasticidade — a capacidade dos neurônios de formar novas conexões e reorganizar circuitos — é a base da recuperação da dependência.
Pesquisas recentes mostram que:
- Meditação mindfulness por 8 semanas pode aumentar a espessura cortical no PFC em até 5%, fortalecendo os circuitos de controle executivo
- Terapia cognitivo-comportamental (TCC) produz mudanças mensuráveis na atividade do PFC visíveis em ressonância magnética funcional após apenas 12 sessões
- Ambientes enriquecidos (social, cognitivo, físico) aceleram a degradação natural da DeltaFosB e promovem a formação de novas conexões saudáveis
- Sono adequado (7-9 horas por noite) é crucial para a consolidação de novos padrões neurais que substituem os circuitos aditivos
- Dieta rica em ômega-3 (peixes, sementes de linhaça) facilita a reparação das membranas neuronais danificadas pelo estresse oxidativo da cocaína
Cronograma de Recuperação Neural
Com base na pesquisa de 2026, os cientistas podem agora estimar com mais precisão o tempo de recuperação de diferentes aspectos da função cerebral:
| Função Cerebral | Início da Recuperação | Recuperação Parcial | Recuperação Substancial |
|---|---|---|---|
| Sensibilidade à dopamina | 2-4 semanas | 3-6 meses | 12-18 meses |
| Controle de impulsos (PFC) | 1-2 meses | 6-12 meses | 18-24 meses |
| Degradação da DeltaFosB | Imediata (lenta) | 2-4 meses | 6-8 meses |
| Reversão epigenética (histonas) | 3-6 meses | 12-18 meses | 24-36 meses |
| Espinhas dendríticas extras | 1-2 meses | 4-6 meses | 8-12 meses |
| Função cognitiva global | 1-3 meses | 6-12 meses | 18-36 meses |
Esses dados são ao mesmo tempo desafiadores e esperançosos: a recuperação é possível, mas exige tempo, suporte e, idealmente, tratamento multidisciplinar continuado.
Prevenção: Lições da Neurociência
A compreensão dos mecanismos moleculares da dependência também informa estratégias de prevenção mais eficazes:
Educação baseada em ciência: Explicar como a cocaína altera fisicamente o cérebro é mais eficaz do que campanhas moral moralizantes. Jovens respondem melhor a fatos neurocientíficos do que a apelos emocionais.
Identificação de fatores de risco genéticos: Variações no gene do receptor de dopamina D2 (DRD2) e no gene do transportador de dopamina (DAT1) aumentam a vulnerabilidade à dependência. Testes genéticos podem identificar indivíduos em risco.
Intervenção precoce: Como a DeltaFosB se acumula progressivamente, interromper o uso nos primeiros estágios é exponencialmente mais eficaz do que tratar dependência crônica.
Saúde mental integrada: Depressão, ansiedade e TDAH são fatores de risco significativos para dependência. Tratar essas condições reduz a vulnerabilidade.
Políticas públicas baseadas em evidência: Programas de redução de danos e acesso a tratamento baseado em neurociência são mais eficazes do que abordagens puramente punitivas.
A História da Pesquisa sobre Dependência
O entendimento do vício como doença cerebral passou por uma transformação radical ao longo do último século:
- 1914: A Lei Harrison nos EUA criminaliza o uso de cocaína, tratando-o como questão moral e criminal
- 1950-1960: Primeiros estudos com animais mostram que ratos preferem cocaína à comida
- 1988: O neurocientista Nora Volkow começa a usar PET scans para mostrar que cérebros de dependentes são fisicamente diferentes
- 1997: Alan Leshner publica artigo seminal no Science: "Addiction Is a Brain Disease"
- 2001: Eric Nestler identifica o papel da DeltaFosB na dependência
- 2013: O DSM-5 reclassifica "abuso de substâncias" como "transtorno por uso de substâncias" — reconhecendo oficialmente como condição médica
- 2026: A descoberta da calreticulina completa o quadro molecular da dependência
Cada uma dessas etapas representou uma ampliação crucial na compreensão do vício, transformando-o gradualmente de pecado em crime, de crime em desordem comportamental, e de desordem em doença neurológica com mecanismos moleculares bem definidos. A pesquisa de 2026 é, sem dúvida, um dos avanços mais significativos nessa trajetória, oferecendo pela primeira vez alvos terapêuticos específicos para intervenção farmacológica precisa contra a dependência de cocaína.
Conclusão: A Dependência É Uma Doença — E Agora Sabemos Exatamente Como Ela Funciona
A descoberta do mecanismo DeltaFosB-calreticulina representa um salto paradigmático na compreensão científica da dependência de cocaína. Pela primeira vez, temos uma visão detalhada e molecular de como a droga reprograma o cérebro, criando vulnerabilidades que persistem muito além do período de uso ativo.
Essa compreensão não diminui a responsabilidade individual, mas contextualiza a luta contra a dependência de forma mais humana e científica. A recaída não é fraqueza — é biologia. E agora que conhecemos o mecanismo, podemos finalmente começar a desenvolver ferramentas para combatê-lo.
2026 pode ser o ano em que deixamos de tratar a dependência como crime moral e passamos a tratá-la como o que ela realmente é: uma doença neurológica tratável. Com alvos moleculares bem definidos como a calreticulina, a comunidade científica finalmente tem as ferramentas para desenvolver medicamentos específicos que podem mudar a vida de milhões de pessoas em todo o mundo que sofrem com a dependência de cocaína e seus derivados.
Fontes e Referências
- Michigan State University. "How cocaine rewires the brain: DeltaFosB and calreticulin mechanism." Março 2026.
- Nature Neuroscience. "Calreticulin amplifies DeltaFosB-mediated epigenetic remodeling in nucleus accumbens." 2026.
- National Institute on Drug Abuse (NIDA). "Understanding Drug Addiction and Dependence." drugabuse.gov
- UNODC World Drug Report 2025.
- Nestler, E.J. "Molecular mechanisms of drug addiction." Journal of Neuroscience, 2013.





