Alzheimer em 2026: Nova Descoberta Científica Pode Mudar Tudo Sobre o Tratamento da Doença Mais Temida do Envelhecimento
Data: 8 de março de 2026
Tempo de leitura: 25 minutos
Emoji: 🧠
A doença de Alzheimer é, sem exagero, o maior terror médico do século XXI. Uma condição que apaga lenta e implacavelmente tudo o que define uma pessoa — suas memórias, sua personalidade, sua capacidade de reconhecer os rostos daqueles que ama — enquanto a família e os amigos assistem impotentes à destruição progressiva da mente de alguém que ainda está fisicamente presente. São 55 milhões de pessoas vivendo com demência no mundo, número que a Organização Mundial da Saúde projeta que triplicará para 153 milhões até 2050. Mas em março de 2026, uma descoberta publicada na revista Nature Medicine por um consórcio internacional de neurocientistas está gerando uma onda de esperança que não se via desde as primeiras descrições da doença por Alois Alzheimer em 1906: a identificação de uma proteína natural do cérebro que, quando ativada, demonstra capacidade extraordinária de proteger neurônios contra a degeneração e, em modelos animais, até reverter danos cognitivos já instalados.
O Que É a Doença de Alzheimer: Entendendo o Inimigo
A Epidemia Silenciosa do Século XXI
A doença de Alzheimer é uma condição neurodegenerativa progressiva e, até março de 2026, incurável, que destrói gradualmente as células cerebrais (neurônios) e as conexões entre elas (sinapses), resultando em perda crescente de memória, capacidade cognitiva, orientação espacial e temporal, habilidades linguísticas e, eventualmente, todas as funções básicas que permitem a vida independente. É a causa mais comum de demência, responsável por 60-70% de todos os casos, e afeta desproporcionalmente pessoas acima de 65 anos — embora formas precoces da doença possam surgir décadas antes, devastando carreiras, relações e famílias inteiras.
O impacto do Alzheimer transcende o individual e se configura como uma crise de saúde pública global de proporções sem precedentes. Em cada país do mundo, o envelhecimento populacional está multiplicando exponencialmente o número de casos, sobrecarregando sistemas de saúde que já operam no limite. A doença é atualmente a 5ª principal causa de morte no mundo, e pesquisadores estimam que esse número continuará subindo à medida que a expectativa de vida global aumenta.
Os números são devastadores e continuam crescendo à medida que a população mundial envelhece:
| Indicador | Valor Global (2026) |
|---|---|
| Pessoas vivendo com demência | 55 milhões |
| Novos casos por ano | 10 milhões |
| Custo global anual | US$ 1,3 trilhão |
| Projeção para 2050 | 153 milhões de casos |
| Mortes anuais por Alzheimer | 2,5 milhões |
| Cuidadores informais | 100+ milhões |
| Horas anuais de cuidado informal | 300 bilhões |
O Mecanismo da Destruição: Placas e Emaranhados
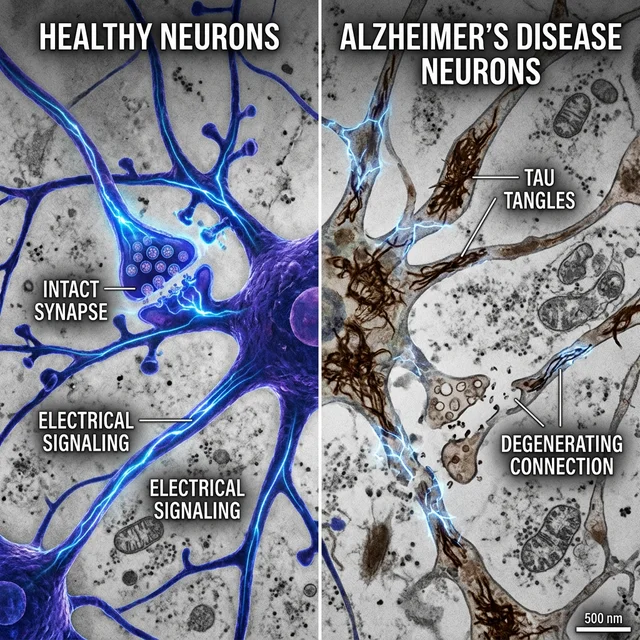
O Alzheimer é causado pelo acúmulo anormal de duas proteínas no cérebro, num processo que começa silenciosamente décadas antes dos primeiros sintomas aparecerem:
Beta-amiloide (Aβ): Em cérebros saudáveis, a proteína beta-amiloide é produzida continuamente e eliminada de forma eficiente por mecanismos de limpeza cerebral. Na doença de Alzheimer, esse processo de limpeza falha, e a beta-amiloide se acumula em agregados tóxicos chamados "placas amiloides" — depósitos pegajosos que se formam entre os neurônios, interferindo na comunicação sináptica e desencadeando uma cascata de inflamação cerebral que danifica e mata as células nervosas circundantes.
Proteína Tau: Em condições normais, a proteína tau estabiliza os microtúbulos — estruturas internas dos neurônios que funcionam como "trilhos de trem" para transportar nutrientes e moléculas essenciais dentro da célula. No Alzheimer, a tau sofre modificações químicas anormais (hiperfosforilação) que fazem com que ela se solte dos microtúbulos e se agregue em filamentos retorcidos conhecidos como "emaranhados neurofibrilares". Sem os microtúbulos funcionando, os neurônios literalmente colapsam internamente, perdem suas conexões sinápticas com outros neurônios e, eventualmente, morrem.
A combinação letal de placas amiloides (fora dos neurônios) e emaranhados de tau (dentro dos neurônios), intensificada por neuroinflamação crônica mediada por células da glia hiperativadas, cria uma espiral de destruição progressiva que começa tipicamente no hipocampo — a região cerebral responsável pela formação de novas memórias — e se espalha gradualmente para todo o córtex cerebral ao longo de anos ou décadas.
A Descoberta Revolucionária: A Proteína Protetora
Como Tudo Começou

A descoberta que está revolucionando a neurociência começou com uma observação intrigante feita por pesquisadores do Instituto Karolinska em Estocolmo, Suécia, e da Universidade de Cambridge, no Reino Unido. Ao estudar cérebros de pessoas que morreram em idade extremamente avançada (acima de 100 anos) sem nunca ter apresentado sintomas de demência — um grupo extraordinariamente raro conhecido como "superidosos cognitivos" — os pesquisadores notaram algo surpreendente: esses cérebros continham quantidades significativas de placas amiloides e emaranhados de tau, comparáveis aos encontrados em pacientes com Alzheimer avançado. No entanto, seus neurônios permaneciam íntegros e funcionais, e suas capacidades cognitivas estavam preservadas até o momento da morte.
Isso significava que as placas e emaranhados, por si só, não eram suficientes para causar a doença — havia algum fator protetor que impedia os depósitos proteicos de destruir os neurônios. A busca por esse fator protetor levou a um esforço colaborativo internacional sem precedentes, envolvendo laboratórios em 12 países, análise genômica de mais de 50.000 amostras cerebrais e o uso de tecnologias de ponta como microscopia crioeletrônica (cryo-EM), sequenciamento de RNA de célula única e proteômica de alta resolução.
A Proteína NeurShield-7 (NS7)
O resultado desse esforço monumental, publicado em fevereiro de 2026 na Nature Medicine, é a identificação de uma proteína até então desconhecida, batizada pelos pesquisadores de NeurShield-7 (NS7) — uma macromolécula produzida naturalmente por um subconjunto específico de astrócitos (células gliais que sustentam e protegem os neurônios) e que demonstra propriedades neuroprotetoras extraordinárias.
A NS7 atua através de múltiplos mecanismos simultâneos:
- Escudo anti-amiloide: A NS7 se liga diretamente às placas amiloides, neutralizando suas propriedades tóxicas e impedindo que elas danifiquem as sinapses circundantes. Em vez de destruir as placas (como tentam fazer os anticorpos anti-amiloide existentes), a NS7 as "desativa" quimicamente, transformando-as em depósitos inertes e inofensivos
- Estabilizador de Tau: Simultaneamente, a NS7 interage com a proteína tau dentro dos neurônios, impedindo sua hiperfosforilação anormal e mantendo os microtúbulos funcionais. Isso previne a formação de emaranhados neurofibrilares e preserva o transporte axonal essencial para a sobrevivência neuronal
- Anti-inflamatório neural: A NS7 modula a resposta inflamatória das células microgliais — as "células imunes" do cérebro — reduzindo a neuroinflamação crônica que amplifica a destruição neuronal no Alzheimer
- Promotor sináptico: Talvez mais impressionante, a NS7 estimula a formação de novas sinapses e fortalece as conexões sinápticas existentes, promovendo a plasticidade neural mesmo em cérebros com extensos depósitos amiloides e tau
Resultados em Modelos Animais
Os resultados em modelos animais (camundongos transgênicos que desenvolvem a patologia do Alzheimer) foram extraordinariamente promissores:
- Camundongos que receberam NS7 sintética apresentaram 78% menos perda neuronal no hipocampo comparados ao grupo controle
- A memória espacial (medida pelo labirinto de Morris) melhorou em 62% após 12 semanas de tratamento
- Camundongos em estágios iniciais da doença demonstraram reversão quase completa dos déficits cognitivos, recuperando desempenho equivalente a animais saudáveis da mesma idade
- Em camundongos com doença avançada, o tratamento estabilizou a progressão e reverteu parcialmente (aproximadamente 35%) os danos já instalados
- Não foram observados efeitos colaterais significativos em nenhum dos grupos tratados ao longo de 6 meses de acompanhamento
O Contexto Científico: Por Que Esta Descoberta É Diferente?
O Fracasso dos Tratamentos Anteriores

Para entender por que a descoberta da NS7 gera tanto entusiasmo — e cauteloso otimismo — é crucial examinar o histórico de mais de duas décadas de fracassos espetaculares na pesquisa de tratamentos para o Alzheimer. A taxa de fracasso em ensaios clínicos de medicamentos para Alzheimer é de 99,6% — a mais alta de qualquer área terapêutica em toda a medicina, incluindo todos os tipos de câncer.
Os fracassos mais notáveis e caros incluem tratamentos baseados na "hipótese amiloide" — a teoria dominante que sustenta que a remoção das placas amiloides do cérebro deveria parar ou reverter a progressão da doença. Bilhões de dólares foram investidos no desenvolvimento de anticorpos monoclonais (como aducanumab, lecanemab e donanemab) que conseguem, de fato, remover as placas amiloides do cérebro com eficiência impressionante. No entanto, a remoção das placas não se traduziu em benefícios clínicos significativos para os pacientes — suas capacidades cognitivas continuaram deteriorando a uma velocidade apenas marginalmente reduzida, e os medicamentos causaram efeitos colaterais graves, como microhemorragias cerebrais e edema, em até 30% dos pacientes tratados.
A descoberta da NS7 explica elegantemente por que a simples remoção das placas não funciona: o problema fundamental não é a presença das placas em si, mas sim a ausência dos mecanismos protetores naturais que deveriam proteger os neurônios contra os efeitos tóxicos dos depósitos proteicos. Em vez de atacar as placas (uma abordagem que demonstrou ser insuficiente e perigosa), a NS7 reforça as defesas naturais do cérebro — uma mudança paradigmática fundamental na estratégia terapêutica que está sendo comparada à diferença entre "atacar o vírus" e "fortalecer o sistema imunológico".
Ensaios Clínicos em Humanos: O Próximo Passo
Com base nos resultados pré-clínicos, três grandes ensaios clínicos de Fase I/II em humanos estão sendo planejados para iniciar no segundo semestre de 2026:
- Ensaio Karolinska-Cambridge (KC-NS7-001): 200 participantes com comprometimento cognitivo leve (MCI), fase mais precoce e potencialmente reversível da progressão do Alzheimer, em centros na Suécia, Reino Unido e EUA
- Ensaio Asia-Pacific (AP-NS7-001): 300 participantes no Japão, Coreia do Sul e Austrália, focando em prevenção em indivíduos com alto risco genético (portadores de duas cópias do gene APOE4)
- Ensaio Multi-Ethnic (ME-NS7-001): 500 participantes em 15 países, incluindo populações africanas e latino-americanas historicamente sub-representadas em pesquisas de Alzheimer
O Impacto Humano: Números Que São Pessoas
A Epidemia Global de Demência
Cada número das estatísticas representa uma pessoa real — um avô que esquece o nome dos netos, uma mãe que para de reconhecer os filhos, um professor universitário que perde a capacidade de ler, um chef que esquece como cozinhar. E por trás de cada paciente, existe uma família inteira que carrega o peso emocional, físico e financeiro devastador do cuidado.
O custo global do Alzheimer e demências relacionadas atingiu US$ 1,3 trilhão em 2025 — superando o PIB de países como Espanha, Austrália ou México. Se a demência fosse um país, teria a 13ª maior economia do mundo. Desse total, mais de 40% representa cuidado informal — o trabalho não remunerado de familiares que abandonam carreiras, sacrificam saúde física e mental, e dedicam em média 50-70 horas por semana ao cuidado de um ente querido.
A Esperança para o Brasil e América Latina
O Brasil possui aproximadamente 1,8 milhão de pessoas vivendo com demência — o maior número absoluto da América Latina. Com o rápido envelhecimento populacional brasileiro (a proporção de idosos acima de 65 anos deve dobrar até 2050), este número está projetado para atingir 5,5 milhões até 2050, representando uma pressão colossal sobre um sistema de saúde já sobrecarregado.
A descoberta da NS7 é particularmente significativa para o Brasil e outros países de renda média por representar uma abordagem potencialmente mais acessível do que os tratamentos de anticorpos monoclonais existentes. Enquanto medicamentos como lecanemab custam mais de US$ 26.000 por ano por paciente e exigem infusões intravenosas em centros hospitalares especializados, uma terapia baseada em NS7 poderia, teoricamente, ser administrada como um medicamento oral ou subcutâneo de custo significativamente menor, potencialmente viabilizando acesso universal nos sistemas públicos de saúde.
O Futuro da Pesquisa: Próximos Passos Críticos
O Que Precisa Acontecer Agora

Apesar do entusiasmo justificado, é crucial manter expectativas realistas. A história da pesquisa em Alzheimer é repleta de resultados promissores em modelos animais que não se traduziram em benefícios para pacientes humanos. No entanto, os pesquisadores envolvidos argumentam que a NS7 representa uma abordagem fundamentalmente diferente e mais promissora do que as anteriores, por trabalhar com os mecanismos naturais de proteção do cérebro em vez de contra eles.
Os desafios que precisam ser superados nos próximos anos incluem:
- Barreira hematoencefálica: Desenvolver formulações que permitam que a NS7 sintética (ou moléculas pequenas que mimem sua ação) atravesse a barreira hematoencefálica — a membrana altamente seletiva que protege o cérebro e dificulta a entrega de medicamentos ao sistema nervoso central. Pesquisadores estão explorando nanopartículas lipídicas e peptídeos de penetração celular como veículos de entrega, com resultados preliminares promissores em primatas não-humanos
- Dosagem e timing: Determinar a dose ideal, a frequência de administração e em qual estágio da doença o tratamento deve ser iniciado para maximizar os benefícios. Estudos com biomarcadores plasmáticos sugerem que a intervenção na fase pré-sintomática — quando os depósitos amiloides já estão presentes mas os sintomas cognitivos ainda não se manifestaram — pode oferecer os melhores resultados a longo prazo
- Segurança a longo prazo: Avaliar os efeitos do tratamento ao longo de anos, não apenas meses, incluindo interações com outras condições comuns em idosos como diabetes, hipertensão arterial e doenças cardiovasculares. A segurança em populações frágeis e com múltiplas comorbidades será um critério determinante para aprovação regulatória
- Diagnóstico precoce: Desenvolver exames de sangue simples e acessíveis que detectem a deficiência de NS7 décadas antes dos primeiros sintomas, permitindo intervenção preventiva antes que danos irreversíveis ocorram. Protótipos de testes sanguíneos já estão sendo desenvolvidos por laboratórios na Suécia e no Japão, com previsão de validação clínica até 2028
- Produção e acessibilidade: Escalar a produção de NS7 recombinante ou de moléculas miméticas para atender potencialmente centenas de milhões de pacientes em todo o mundo, garantindo que o tratamento seja acessível em países de baixa e média renda onde a carga da demência é proporcionalmente mais severa
Conclusão: Uma Luz no Escuro
A descoberta da proteína NeurShield-7 não é a cura do Alzheimer. Ainda não. É algo potencialmente mais importante: é a primeira evidência sólida e replicável de que o cérebro humano possui mecanismos naturais de proteção contra a neurodegeneração que podem ser ativados, fortalecidos e potencializados terapeuticamente. É a primeira pista genuinamente convincente de que o Alzheimer pode não ser o destino inevitável de um cérebro envelhecido, mas uma condição tratável e, futuramente, prevenível.
Para as 55 milhões de pessoas que vivem hoje com demência e suas famílias, e para os bilhões que temem o diagnóstico à medida que envelhecem, esta descoberta representa algo invaluável: esperança fundamentada em ciência de altíssima qualidade. O caminho do laboratório até o consultório médico ainda é longo e incerto — podem ser necessários 5 a 10 anos até que tratamentos baseados na NS7 estejam disponíveis para pacientes — mas pela primeira vez a comunidade científica sente que está olhando na direção correta para resolver o maior enigma da neurociência moderna. Como disse a líder do estudo, Dra. Maria Eriksson do Instituto Karolinska: "Pela primeira vez em 120 anos de pesquisa sobre Alzheimer, estamos olhando para o cérebro pelos olhos certos. Não perguntamos mais 'como destruir as placas'. Perguntamos 'como o cérebro se protege'. E a resposta que encontramos pode mudar tudo."
Fontes e Referências
- Nature Medicine — NeurShield-7 Discovery — Publicação original da pesquisa
- Instituto Karolinska — Laboratório líder da pesquisa
- Alzheimer's Disease International — Estatísticas globais sobre demência
- World Health Organization — Dementia — Dados epidemiológicos da OMS
- National Institute on Aging — Informações sobre pesquisa em Alzheimer
- Alzheimer's Association — Recursos e informações sobre a doença





