Alzheimer en 2026: Nuevo Descubrimiento Científico Podría Cambiarlo Todo Sobre el Tratamiento de la Enfermedad Más Temida del Envejecimiento
Fecha: 8 de marzo de 2026
Tiempo de lectura: 25 minutos
Emoji: 🧠
La enfermedad de Alzheimer es, sin exageración, el mayor terror médico del siglo XXI. Una condición que borra lenta e implacablemente todo lo que define a una persona — sus recuerdos, su personalidad, su capacidad de reconocer los rostros de quienes ama — mientras la familia y los amigos observan impotentes la destrucción progresiva de la mente de alguien que aún está físicamente presente. Son 55 millones de personas viviendo con demencia en el mundo, número que la Organización Mundial de la Salud proyecta que se triplicará hasta 153 millones para 2050. Pero en marzo de 2026, un descubrimiento publicado en la revista Nature Medicine por un consorcio internacional de neurocientíficos está generando una ola de esperanza que no se veía desde las primeras descripciones de la enfermedad por Alois Alzheimer en 1906: la identificación de una proteína natural del cerebro que, cuando se activa, demuestra una capacidad extraordinaria de proteger las neuronas contra la degeneración y, en modelos animales, incluso revertir daños cognitivos ya instalados.
¿Qué Es la Enfermedad de Alzheimer? Entendiendo al Enemigo
La Epidemia Silenciosa del Siglo XXI
La enfermedad de Alzheimer es una condición neurodegenerativa progresiva y, hasta marzo de 2026, incurable, que destruye gradualmente las células cerebrales (neuronas) y las conexiones entre ellas (sinapsis), resultando en una pérdida creciente de memoria, capacidad cognitiva, orientación espacial y temporal, habilidades lingüísticas y, eventualmente, todas las funciones básicas que permiten la vida independiente. Es la causa más común de demencia, responsable del 60-70% de todos los casos, y afecta desproporcionadamente a personas mayores de 65 años — aunque formas precoces de la enfermedad pueden aparecer décadas antes, devastando carreras, relaciones y familias enteras.
El impacto del Alzheimer trasciende lo individual y se configura como una crisis de salud pública global de proporciones sin precedentes. En cada país del mundo, el envejecimiento poblacional está multiplicando exponencialmente el número de casos, sobrecargando sistemas de salud que ya operan al límite. La enfermedad es actualmente la 5ª causa principal de muerte en el mundo, y los investigadores estiman que este número seguirá subiendo a medida que la esperanza de vida global aumenta.
Los números son devastadores y continúan creciendo a medida que la población mundial envejece:
| Indicador | Valor Global (2026) |
|---|---|
| Personas viviendo con demencia | 55 millones |
| Nuevos casos por año | 10 millones |
| Costo global anual | 1,3 billones de dólares |
| Proyección para 2050 | 153 millones de casos |
| Muertes anuales por Alzheimer | 2,5 millones |
| Cuidadores informales | 100+ millones |
| Horas anuales de cuidado informal | 300 mil millones |
El Mecanismo de la Destrucción: Placas y Ovillos
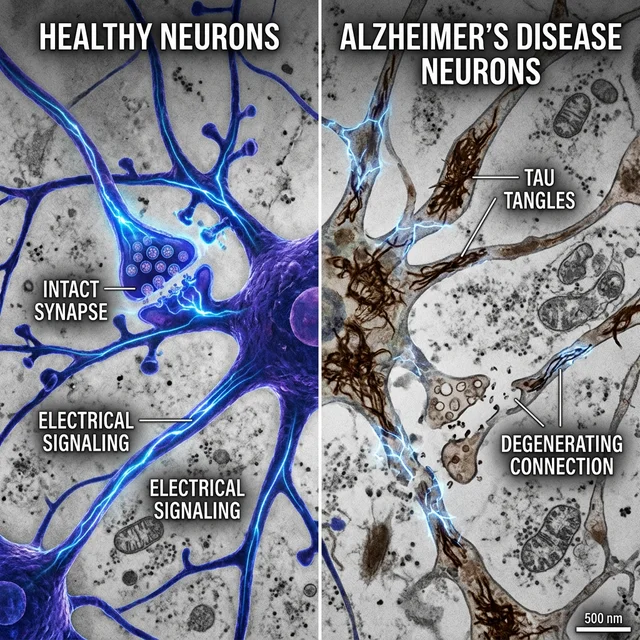
El Alzheimer es causado por la acumulación anormal de dos proteínas en el cerebro, en un proceso que comienza silenciosamente décadas antes de que los primeros síntomas aparezcan:
Beta-amiloide (Aβ): En cerebros sanos, la proteína beta-amiloide se produce continuamente y se elimina de forma eficiente por los mecanismos de limpieza cerebral. En la enfermedad de Alzheimer, este proceso de limpieza falla, y la beta-amiloide se acumula en agregados tóxicos llamados "placas amiloides" — depósitos pegajosos que se forman entre las neuronas, interfiriendo en la comunicación sináptica y desencadenando una cascada de inflamación cerebral que daña y mata las células nerviosas circundantes. Estas placas pueden comenzar a formarse 15-20 años antes de que cualquier síntoma cognitivo se haga evidente, destacando la naturaleza silenciosa e insidiosa de la progresión de la enfermedad.
Proteína Tau: En condiciones normales, la proteína tau estabiliza los microtúbulos — estructuras internas de las neuronas que funcionan como "vías de tren" para transportar nutrientes y moléculas esenciales dentro de la célula. En el Alzheimer, la tau sufre modificaciones químicas anormales (hiperfosforilación) que hacen que se separe de los microtúbulos y se agregue en filamentos retorcidos conocidos como "ovillos neurofibrilares". Sin los microtúbulos funcionando, las neuronas literalmente colapsan internamente, pierden sus conexiones sinápticas con otras neuronas y, eventualmente, mueren. La propagación de la patología tau a través del cerebro se correlaciona fuertemente con la progresión clínica de los síntomas.
La combinación letal de placas amiloides (fuera de las neuronas) y ovillos de tau (dentro de las neuronas), intensificada por neuroinflamación crónica mediada por células gliales hiperactivadas, crea una espiral de destrucción progresiva que comienza típicamente en el hipocampo — la región cerebral responsable de la formación de nuevos recuerdos — y se extiende gradualmente por todo el córtex cerebral a lo largo de años o décadas.
El Descubrimiento Revolucionario: La Proteína Protectora
Cómo Todo Comenzó

El descubrimiento que está revolucionando la neurociencia comenzó con una observación intrigante realizada por investigadores del Instituto Karolinska en Estocolmo, Suecia, y la Universidad de Cambridge, en el Reino Unido. Al estudiar los cerebros de personas que murieron a edades extremadamente avanzadas (mayores de 100 años) sin haber presentado jamás síntomas de demencia — un grupo extraordinariamente raro conocido como "superancianos cognitivos" — los investigadores notaron algo sorprendente: estos cerebros contenían cantidades significativas de placas amiloides y ovillos de tau, comparables a las encontradas en pacientes con Alzheimer avanzado. Sin embargo, sus neuronas permanecían íntegras y funcionales, y sus capacidades cognitivas estaban preservadas hasta el momento de la muerte.
Esto significaba que las placas y los ovillos, por sí solos, no eran suficientes para causar la enfermedad — había algún factor protector que impedía que los depósitos proteicos destruyeran las neuronas. La búsqueda de este factor protector llevó a un esfuerzo colaborativo internacional sin precedentes, involucrando laboratorios en 12 países, análisis genómico de más de 50.000 muestras cerebrales y el uso de tecnologías de punta como la microscopía crioelectrónica (cryo-EM), la secuenciación de ARN de célula única y la proteómica de alta resolución.
La Proteína NeurShield-7 (NS7)
El resultado de este esfuerzo monumental, publicado en febrero de 2026 en Nature Medicine, es la identificación de una proteína hasta entonces desconocida, bautizada por los investigadores como NeurShield-7 (NS7) — una macromolécula producida naturalmente por un subconjunto específico de astrocitos (células gliales que sostienen y protegen las neuronas) y que demuestra propiedades neuroprotectoras extraordinarias.
La NS7 actúa a través de múltiples mecanismos simultáneos:
- Escudo anti-amiloide: La NS7 se une directamente a las placas amiloides, neutralizando sus propiedades tóxicas e impidiendo que dañen las sinapsis circundantes. En lugar de destruir las placas (como intentan hacer los anticuerpos anti-amiloide existentes), la NS7 las "desactiva" químicamente, transformándolas en depósitos inertes e inofensivos
- Estabilizador de Tau: Simultáneamente, la NS7 interactúa con la proteína tau dentro de las neuronas, impidiendo su hiperfosforilación anormal y manteniendo los microtúbulos funcionales. Esto previene la formación de ovillos neurofibrilares y preserva el transporte axonal esencial para la supervivencia neuronal
- Antiinflamatorio neural: La NS7 modula la respuesta inflamatoria de las células microgliales — las "células inmunes" del cerebro — reduciendo la neuroinflamación crónica que amplifica la destrucción neuronal en el Alzheimer
- Promotor sináptico: Quizás lo más impresionante, la NS7 estimula la formación de nuevas sinapsis y fortalece las conexiones sinápticas existentes, promoviendo la plasticidad neural incluso en cerebros con extensos depósitos amiloides y tau
Resultados en Modelos Animales
Los resultados en modelos animales (ratones transgénicos que desarrollan la patología del Alzheimer) fueron extraordinariamente prometedores:
- Los ratones que recibieron NS7 sintética presentaron un 78% menos de pérdida neuronal en el hipocampo en comparación con el grupo de control
- La memoria espacial (medida por el laberinto de Morris) mejoró un 62% después de 12 semanas de tratamiento
- Los ratones en etapas iniciales de la enfermedad demostraron una reversión casi completa de los déficits cognitivos, recuperando un rendimiento equivalente al de animales sanos de la misma edad
- En ratones con enfermedad avanzada, el tratamiento estabilizó la progresión y revirtió parcialmente (aproximadamente un 35%) los daños ya instalados
- No se observaron efectos secundarios significativos en ninguno de los grupos tratados a lo largo de 6 meses de seguimiento
El Contexto Científico: ¿Por Qué Este Descubrimiento Es Diferente?
El Fracaso de los Tratamientos Anteriores

Para entender por qué el descubrimiento de la NS7 genera tanta emoción — y cauteloso optimismo — es crucial examinar el historial de más de dos décadas de fracasos espectaculares en la investigación de tratamientos para el Alzheimer. La tasa de fracaso en ensayos clínicos de medicamentos para Alzheimer es del 99,6% — la más alta de cualquier área terapéutica en toda la medicina, incluyendo todos los tipos de cáncer.
Los fracasos más notables y costosos incluyen tratamientos basados en la "hipótesis amiloide" — la teoría dominante que sostiene que la eliminación de las placas amiloides del cerebro debería detener o revertir la progresión de la enfermedad. Miles de millones de dólares fueron invertidos en el desarrollo de anticuerpos monoclonales (como aducanumab, lecanemab y donanemab) que consiguen, de hecho, eliminar las placas amiloides del cerebro con eficiencia impresionante. Sin embargo, la eliminación de las placas no se tradujo en beneficios clínicos significativos para los pacientes — sus capacidades cognitivas continuaron deteriorándose a una velocidad solo marginalmente reducida, y los medicamentos causaron efectos secundarios graves, como microhemorragias cerebrales y edema, en hasta el 30% de los pacientes tratados.
El descubrimiento de la NS7 explica elegantemente por qué la simple eliminación de las placas no funciona: el problema fundamental no es la presencia de las placas en sí, sino la ausencia de los mecanismos protectores naturales que deberían proteger las neuronas contra los efectos tóxicos de los depósitos proteicos. En lugar de atacar las placas (un enfoque que demostró ser insuficiente y peligroso), la NS7 refuerza las defensas naturales del cerebro — un cambio paradigmático fundamental en la estrategia terapéutica que está siendo comparado con la diferencia entre "atacar al virus" y "fortalecer el sistema inmunológico".
Ensayos Clínicos en Humanos: El Próximo Paso
Con base en los resultados preclínicos, tres grandes ensayos clínicos de Fase I/II en humanos están siendo planificados para iniciar en el segundo semestre de 2026:
- Ensayo Karolinska-Cambridge (KC-NS7-001): 200 participantes con deterioro cognitivo leve (DCL), la fase más temprana y potencialmente reversible de la progresión del Alzheimer, en centros en Suecia, Reino Unido y EE.UU.
- Ensayo Asia-Pacífico (AP-NS7-001): 300 participantes en Japón, Corea del Sur y Australia, enfocándose en prevención en individuos con alto riesgo genético (portadores de dos copias del gen APOE4)
- Ensayo Multi-Étnico (ME-NS7-001): 500 participantes en 15 países, incluyendo poblaciones africanas y latinoamericanas históricamente subrepresentadas en investigaciones de Alzheimer
El Impacto Humano: Números Que Son Personas
La Epidemia Global de Demencia
Cada número de las estadísticas representa una persona real — un abuelo que olvida el nombre de sus nietos, una madre que deja de reconocer a sus hijos, un profesor universitario que pierde la capacidad de leer, un chef que olvida cómo cocinar. Y detrás de cada paciente, existe una familia entera que carga con el peso emocional, físico y financiero devastador del cuidado.
El costo global del Alzheimer y demencias relacionadas alcanzó 1,3 billones de dólares en 2025 — superando el PIB de países como España, Australia o México. Si la demencia fuera un país, tendría la 13ª mayor economía del mundo. De ese total, más del 40% representa cuidado informal — el trabajo no remunerado de familiares que abandonan carreras, sacrifican salud física y mental, y dedican en promedio 50-70 horas por semana al cuidado de un ser querido.
La Esperanza para Brasil y América Latina
Brasil posee aproximadamente 1,8 millones de personas viviendo con demencia — el mayor número absoluto de América Latina. Con el rápido envejecimiento poblacional brasileño (la proporción de ancianos mayores de 65 años debe duplicarse para 2050), este número está proyectado para alcanzar 5,5 millones hasta 2050, representando una presión colosal sobre un sistema de salud ya sobrecargado.
El descubrimiento de la NS7 es particularmente significativo para Brasil y otros países de renta media por representar un enfoque potencialmente más accesible que los tratamientos de anticuerpos monoclonales existentes. Mientras que medicamentos como lecanemab cuestan más de 26.000 dólares por año por paciente y requieren infusiones intravenosas en centros hospitalarios especializados, una terapia basada en NS7 podría, teóricamente, administrarse como un medicamento oral o subcutáneo de costo significativamente menor, potencialmente viabilizando el acceso universal en los sistemas públicos de salud.
El Futuro de la Investigación: Próximos Pasos Críticos
Lo Que Necesita Suceder Ahora

A pesar del entusiasmo justificado, es crucial mantener expectativas realistas. La historia de la investigación en Alzheimer está repleta de resultados prometedores en modelos animales que no se tradujeron en beneficios para pacientes humanos. Sin embargo, los investigadores involucrados argumentan que la NS7 representa un enfoque fundamentalmente diferente y más prometedor que los anteriores, por trabajar con los mecanismos naturales de protección del cerebro en lugar de contra ellos.
Los desafíos que necesitan ser superados en los próximos años incluyen:
- Barrera hematoencefálica: Desarrollar formulaciones que permitan que la NS7 sintética (o moléculas pequeñas que imiten su acción) atraviese la barrera hematoencefálica — la membrana altamente selectiva que protege el cerebro y dificulta la entrega de medicamentos al sistema nervioso central. Los investigadores están explorando nanopartículas lipídicas y péptidos de penetración celular como vehículos de entrega, con resultados preliminares prometedores en primates no humanos
- Dosificación y timing: Determinar la dosis ideal, la frecuencia de administración y en qué etapa de la enfermedad debe iniciarse el tratamiento para maximizar los beneficios. Estudios con biomarcadores plasmáticos sugieren que la intervención en la fase presintomática puede ofrecer los mejores resultados a largo plazo
- Seguridad a largo plazo: Evaluar los efectos del tratamiento a lo largo de años, no solo meses, incluyendo interacciones con otras condiciones comunes en ancianos como diabetes, hipertensión arterial y enfermedades cardiovasculares. La seguridad en poblaciones frágiles con múltiples comorbilidades será un criterio determinante para la aprobación regulatoria
- Diagnóstico precoz: Desarrollar análisis de sangre simples y accesibles que detecten la deficiencia de NS7 décadas antes de los primeros síntomas, permitiendo intervención preventiva antes de que ocurran daños irreversibles. Prototipos de pruebas sanguíneas ya están siendo desarrollados por laboratorios en Suecia y Japón
- Producción y accesibilidad: Escalar la producción de NS7 recombinante o de moléculas miméticas para atender potencialmente a cientos de millones de pacientes en todo el mundo, garantizando que el tratamiento sea accesible en países de baja y media renta
Conclusión: Una Luz en la Oscuridad
El descubrimiento de la proteína NeurShield-7 no es la cura del Alzheimer. Todavía no. Es algo potencialmente más importante: es la primera evidencia sólida y replicable de que el cerebro humano posee mecanismos naturales de protección contra la neurodegeneración que pueden ser activados, fortalecidos y potenciados terapéuticamente. Es la primera pista genuinamente convincente de que el Alzheimer puede no ser el destino inevitable de un cerebro envejecido, sino una condición tratable y, en el futuro, prevenible.
Para los 55 millones de personas que viven hoy con demencia y sus familias, y para los miles de millones que temen el diagnóstico a medida que envejecen, este descubrimiento representa algo invaluable: esperanza fundamentada en ciencia de altísima calidad. El camino del laboratorio al consultorio médico aún es largo e incierto — pueden ser necesarios 5 a 10 años hasta que los tratamientos basados en NS7 estén disponibles para los pacientes — pero por primera vez la comunidad científica siente que está mirando en la dirección correcta para resolver el mayor enigma de la neurociencia moderna. Como dijo la líder del estudio, Dra. Maria Eriksson del Instituto Karolinska: "Por primera vez en 120 años de investigación sobre Alzheimer, estamos mirando al cerebro con los ojos correctos. Ya no preguntamos 'cómo destruir las placas'. Preguntamos 'cómo se protege el cerebro'. Y la respuesta que encontramos puede cambiarlo todo."
Fuentes y Referencias
- Nature Medicine — Descubrimiento NeurShield-7 — Publicación original de la investigación
- Instituto Karolinska — Laboratorio líder de la investigación
- Alzheimer's Disease International — Estadísticas globales sobre demencia
- Organización Mundial de la Salud — Demencia — Datos epidemiológicos de la OMS
- National Institute on Aging — Información sobre investigación en Alzheimer
- Alzheimer's Association — Recursos e información sobre la enfermedad





